Transdermale Impfung über 3D-gedruckte Mikronadeln induziert eine starke humorale und zelluläre Immunität
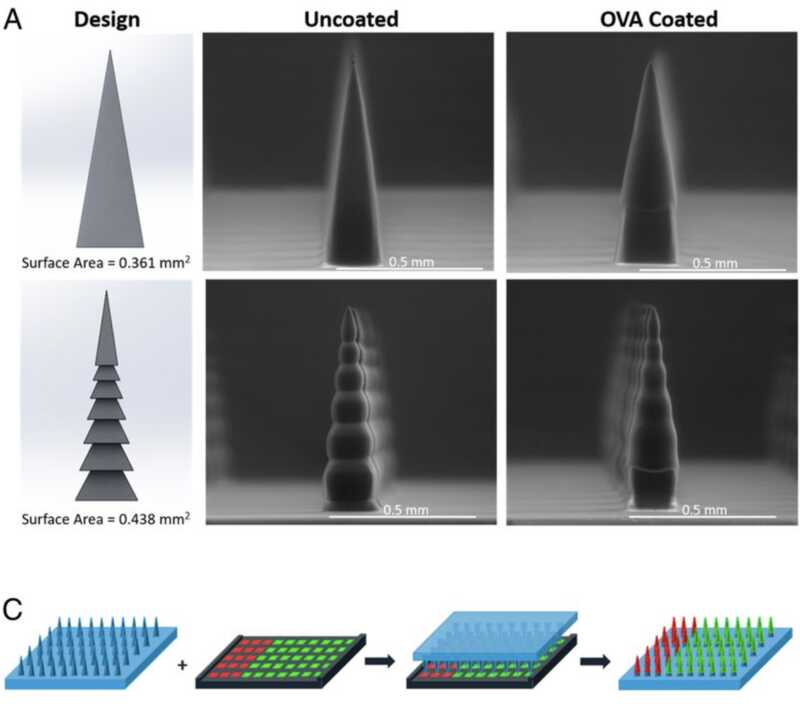
Vaccination is an essential public health measure for infectious disease prevention. The exposure of the immune system to vaccine formulations with the appropriate kinetics is critical for inducing protective immunity. In this work, faceted microneedle arrays were designed and fabricated utilizing a three-dimensional (3D)-printing technique called continuous liquid interface production (CLIP). The faceted microneedle design resulted in increased surface area as compared with the smooth square pyramidal design, ultimately leading to enhanced surface coating of model vaccine components (ovalbumin and CpG). Utilizing fluorescent tags and live-animal imaging, we evaluated in vivo cargo retention and bioavailability in mice as a function of route of delivery. Compared with subcutaneous bolus injection of the soluble components, microneedle transdermal delivery not only resulted in enhanced cargo retention in the skin but also improved immune cell activation in the draining lymph nodes. Furthermore, the microneedle vaccine induced a potent humoral immune response, with higher total IgG (Immunoglobulin G) and a more balanced IgG1/IgG2a repertoire and achieved dose sparing. Furthermore, it elicited T cell responses as characterized by functional cytotoxic CD8+ T cells and CD4+ T cells secreting Th1 (T helper type 1)-cytokines. Taken together, CLIP 3D–printed microneedles coated with vaccine components provide a useful platform for a noninvasive, self-applicable vaccination.
Die Impfung ist eine wesentliche Maßnahme des öffentlichen Gesundheitswesens zur Prävention von Infektionskrankheiten. Die Exposition des Immunsystems gegenüber Impfstoffformulierungen mit der geeigneten Kinetik ist entscheidend für die Induktion einer schützenden Immunität. In dieser Arbeit wurden facettierte Mikronadelfelder entworfen und mit Hilfe einer dreidimensionalen (3D) Drucktechnik hergestellt, die als kontinuierliche Flüssigkeitsschnittstellenproduktion (CLIP) bezeichnet wird. Das facettierte Mikronadeldesign führte zu einer vergrößerten Oberfläche im Vergleich zum glatten quadratischen Pyramidendesign, was letztlich zu einer verbesserten Oberflächenbeschichtung von Modellimpfstoffkomponenten (Ovalbumin und CpG) führte. Mithilfe von fluoreszierenden Markierungen und der Bildgebung bei lebenden Tieren haben wir in vivo die Retention der Ladung und die Bioverfügbarkeit bei Mäusen in Abhängigkeit vom Verabreichungsweg untersucht. Im Vergleich zur subkutanen Bolusinjektion der löslichen Komponenten führte die transdermale Verabreichung über Mikronadeln nicht nur zu einer erhöhten Retention der Ladung in der Haut, sondern auch zu einer verbesserten Aktivierung der Immunzellen in den drainierenden Lymphknoten. Darüber hinaus induzierte der Mikronadel-Impfstoff eine starke humorale Immunantwort mit einem höheren Gesamt-IgG (Immunglobulin G) und einem ausgewogeneren IgG1/IgG2a-Repertoire und erreichte eine geringe Dosis. Darüber hinaus löste es eine T-Zell-Antwort aus, die durch funktionelle zytotoxische CD8+ T-Zellen und CD4+ T-Zellen, die Th1 (T-Helfer Typ 1)-Zytokine sezernieren, gekennzeichnet war. Insgesamt stellen die mit Impfstoffkomponenten beschichteten 3D-gedruckten CLIP-Mikronadeln eine nützliche Plattform für eine nicht-invasive, selbst anwendbare Impfung dar.
We have demonstrated that transdermal delivery of a model vaccine formulation by MNs is superior to subcutaneously or intradermally administered soluble formulation in eliciting potent antibody responses in both initial antigen-specific IgG and the duration of the response. This could be attributed to more efficient and sustained availability of antigen/adjuvant via MN transdermal delivery in the dermal space as well as in the draining lymph nodes where adaptive immunity develops. The viscous coating formulation could also contribute to the slower clearance of cargos. Sustained cargo availability not only favors antigen presentation but also enhances the function of adjuvants that activates innate immune responses to create a local immunocompetent environment at both injection site and dLNs.
Wir haben gezeigt, dass die transdermale Verabreichung einer Modellimpfstoffformulierung durch MNs der subkutan oder intradermal verabreichten löslichen Formulierung überlegen ist, wenn es darum geht, potente Antikörperreaktionen auszulösen, sowohl was die anfänglichen antigenspezifischen IgG als auch die Dauer der Reaktion betrifft. Dies könnte auf die effizientere und dauerhaftere Verfügbarkeit von Antigen/Adjuvans über die transdermale Verabreichung von MN im Hautbereich sowie in den drainierenden Lymphknoten zurückzuführen sein, wo sich die adaptive Immunität entwickelt. Die viskose Beschichtungsformulierung könnte auch zu einer langsameren Freisetzung der Ladung beitragen. Die anhaltende Verfügbarkeit der Ladung begünstigt nicht nur die Antigenpräsentation, sondern verstärkt auch die Funktion von Adjuvantien, die angeborene Immunreaktionen aktivieren, um eine lokale immunkompetente Umgebung sowohl an der Injektionsstelle als auch in den dLN zu schaffen.